天津国晟中源科技有限责任公司
6 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
技术资料/正文
分子蛋白丨实时荧光定量(QPCR)
1332 人阅读发布时间:2024-01-24 10:43
实时荧光定量(QPCR)
实时荧光定量QPCR(Quantitative Real-time PCR)是一种在DNA扩增反应中,以荧光化学物质测每次聚合酶链式反应(PCR)循环后产物总量的方法。它可以通过内部参照物或外部参照物的方法对待测样品中特定DNA序列进行定量分析。
Real-time PCR在PCR扩增过程中通过荧光信号对PCR进行实时检测。由于在PCR扩增的指数阶段,模板的Ct值(阈值周期数)与该模板的起始拷贝数呈线性关系,因此可作为定量分析的依据。通过测量Ct值和标准曲线的比较,可以确定待测样品中特定DNA序列的相对数量或绝对拷贝数。
实时荧光定量QPCR技术具有高灵敏度、高特异性和广泛的动态范围,广泛应用于基因表达分析、病原体检测、基因突变鉴定等领域。它在生物医学研究和临床诊断中发挥着重要作用,是科学研究和医学实践领域可靠的分子生物学工具。
一、实时荧光定量(QPCR)操作流程
(一)、RNA提取
1、组织样本:将新鲜组织切成适当大小后,加入裂解液裂解。每30-50mg组织加入1ml Trizol。
2、全血样本:加入红细胞裂解液至血样中,室温孵育10分钟后离心。弃去上清液,每2-3ml全血样本加入1ml Trizol。
3、细胞样本:悬浮液中的细胞每1×105〜106细胞加入1ml Trizol,混匀后裂解。贴壁生长的细胞可先用胰蛋白酶消化下来后加入Trizol进行裂解。
4、提取RNA:根据Trizol试剂的直接法或离心柱法进行RNA提取。
(二)、反转录
1、检测RNA纯度和完整性:使用紫外分光光度法测定RNA浓度和纯度,以及琼脂糖凝胶电泳评估RNA完整性。
2、反转录:将RNA转录成cDNA,反应条件为42℃孵育40分钟,85℃加热5分钟。
(三)、引物设计
1、引物设计:使用Primer5.0软件设计特异引物。
2、引物设计标准:长度50-180bp,GC含量45-55%,Tm值58-68℃,避免互补和重复结构。
(四)、Q-PCR反应
1、准备反应体系:将cDNA稀释后加入反应体系。
2、扩增循环:按照设定的扩增循环条件进行PCR反应。
3、熔解程序:在扩增循环结束后,进行熔解程序,将产物变性。
4、结果分析:通过荧光信号检测PCR产物的累积量,根据标准曲线计算待测样品中特定DNA序列的相对数量或绝对拷贝数。
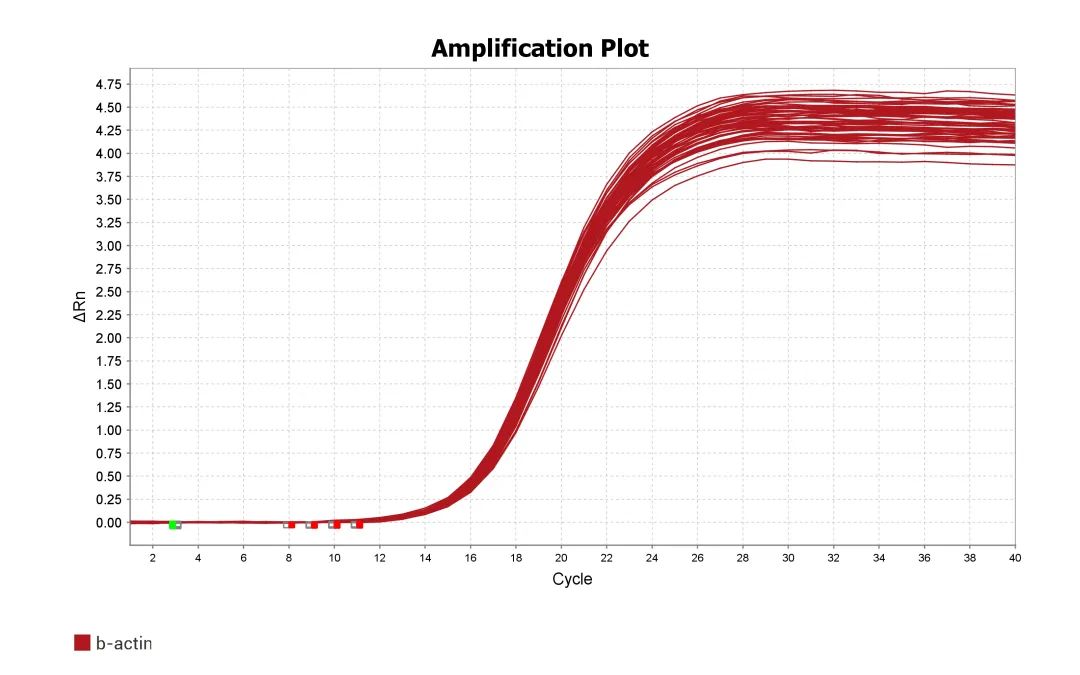
实时扩增曲线图
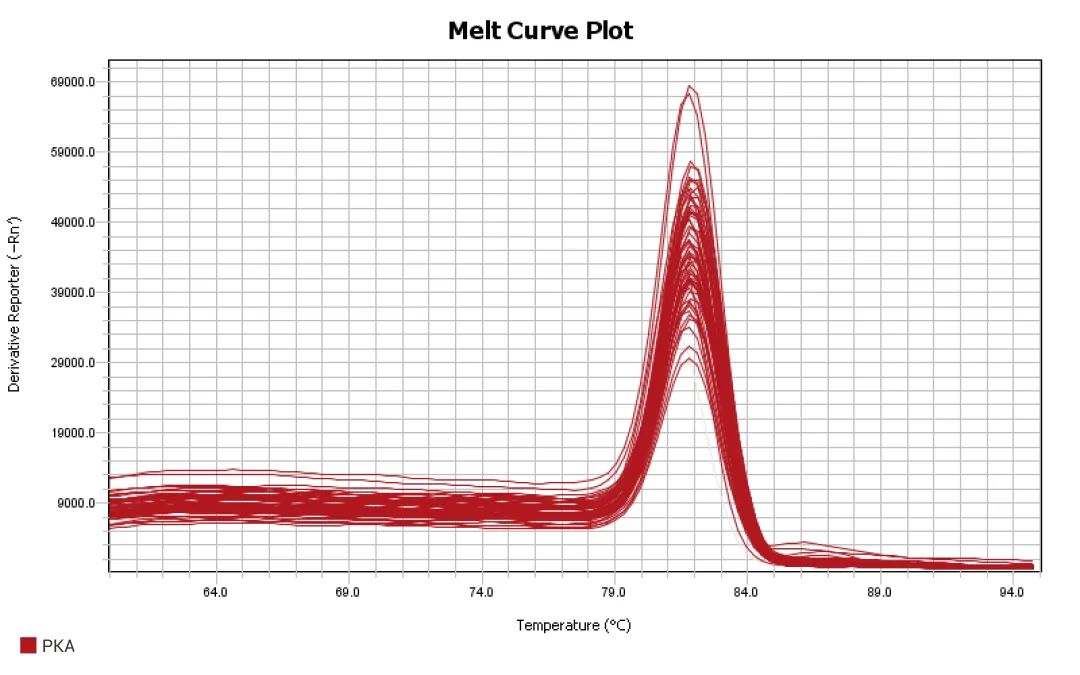
产物溶解曲线图
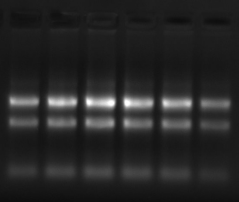
RNA电泳
二、注意事项:
1、RNA提取过程中要注意使用RNase-free试剂和消毒仪器,避免RNA降解。
2、引物设计要考虑特异性和合适的Tm值,避免互补和重复结构。
3、Q-PCR反应中的温度和时间要根据引物和模板的特性进行优化。
4、结果分析时要根据标准曲线计算样品中特定DNA序列的相对数量或绝对拷贝数。
参考文献:
[1]PMA-qPCR快速检测畜禽肉类中沙门氏菌活菌方法的建立 [J] . 刘光富1 ,马骉1 ,付贤树1 . 中国计量大学学报 . 2018,第004期
[2]应用Real Time PCR方法检测病毒灭活去除效率 [J] . 黄亮 ,高婧 ,杜燕华 . 西北大学学报(自然科学版) . 2007,第004期
[3]单核细胞增生性李斯特菌PCR快速检测方法建立及应用 [J] . 巢国祥 ,徐勤 ,周晓辉 . 中国人兽共患病学报 . 2004,第009期
[4]基于活菌内标的单核细胞增生李斯特菌荧光定量PCR方法的建立 [A] . 龙飞 . 2008